کاشکسی یک بیماری سیستمیک است که با کاهش وزن، آتروفی بافت ماهیچه و چربی و التهاب سیستمیک مشخص میشود. کاشکسی یکی از عوارض اصلی و علل مرگ در بیماران سرطانی است. تخمین زده میشود که میزان بروز کاشکسی در بیماران سرطانی میتواند به 25 تا 70 درصد برسد و حدود 9 میلیون نفر در سراسر جهان هر ساله از کاشکسی رنج میبرند که انتظار میرود 80 درصد از آنها ظرف یک سال پس از تشخیص بیماری جان خود را از دست بدهند. علاوه بر این، کاشکسی به طور قابل توجهی بر کیفیت زندگی بیمار (QOL) تأثیر میگذارد و سمیت مرتبط با درمان را تشدید میکند.
مداخله مؤثر در کاشکسی برای بهبود کیفیت زندگی و پیشآگهی بیماران سرطانی از اهمیت بالایی برخوردار است. با این حال، علیرغم پیشرفتهایی در مطالعه مکانیسمهای پاتوفیزیولوژیک کاشکسی، بسیاری از داروهایی که بر اساس مکانیسمهای احتمالی توسعه یافتهاند، تنها تا حدی مؤثر یا بیاثر هستند. در حال حاضر هیچ درمان مؤثری توسط سازمان غذا و داروی ایالات متحده (FDA) تأیید نشده است.
کاشکسی (سندرم لاغری) در بیماران مبتلا به انواع مختلف سرطان بسیار شایع است و اغلب منجر به کاهش وزن، تحلیل عضلات، کاهش کیفیت زندگی، اختلال در عملکرد و کاهش طول عمر میشود. طبق استانداردهای توافقشده بینالمللی، این سندرم چندعاملی به صورت شاخص توده بدنی (BMI، وزن [کیلوگرم] تقسیم بر قد [متر] به توان دو) کمتر از 20 یا در بیماران مبتلا به سارکوپنی، کاهش وزن بیش از 5٪ در شش ماه یا کاهش وزن بیش از 2٪ تعریف میشود. در حال حاضر، هیچ دارویی در ایالات متحده و اروپا به طور خاص برای درمان کاشکسی سرطان تأیید نشده است، که منجر به گزینههای درمانی محدود میشود.
دستورالعملهای اخیر که اولانزاپین با دوز پایین را برای بهبود اشتها و وزن در بیماران مبتلا به سرطان پیشرفته توصیه میکنند، عمدتاً بر اساس نتایج یک مطالعه تک مرکزی هستند. علاوه بر این، استفاده کوتاه مدت از آنالوگهای پروژسترون یا گلوکوکورتیکوئیدها ممکن است مزایای محدودی داشته باشد، اما خطر عوارض جانبی نامطلوب (مانند استفاده از پروژسترون مرتبط با حوادث ترومبوآمبولیک) نیز وجود دارد. آزمایشهای بالینی سایر داروها نتوانستهاند اثربخشی کافی برای کسب تأییدیه قانونی را نشان دهند. اگرچه آنامورین (نسخه خوراکی پپتیدهای آزادکننده هورمون رشد) در ژاپن برای درمان کاشکسی سرطان تأیید شده است، اما این دارو فقط تا حدی ترکیب بدن را افزایش داد، قدرت گرفتن اجسام را بهبود نبخشید و در نهایت توسط سازمان غذا و داروی ایالات متحده (FDA) تأیید نشد. نیاز مبرمی به درمانهای ایمن، مؤثر و هدفمند برای کاشکسی سرطان وجود دارد.
فاکتور تمایز رشد ۱۵ (GDF-15) یک سیتوکین القا شده توسط استرس است که به پروتئین آلفا-مانند گیرنده خانواده فاکتور نوروتروفیک مشتق از گلیا (GFRAL) در مغز خلفی متصل میشود. مسیر GDF-15-GFRAL به عنوان تنظیمکننده اصلی بیاشتهایی و تنظیم وزن شناسایی شده است و در پاتوژنز کاشکسی نقش دارد. در مدلهای حیوانی، GDF-15 میتواند کاشکسی را القا کند و مهار GDF-15 میتواند این علامت را کاهش دهد. علاوه بر این، سطح بالای GDF-15 در بیماران سرطانی با کاهش وزن بدن و توده عضلانی اسکلتی، کاهش قدرت و کاهش بقا همراه است که بر ارزش GDF-15 به عنوان یک هدف درمانی بالقوه تأکید میکند.
پونسگروماب (PF-06946860) یک آنتیبادی مونوکلونال انسانی بسیار گزینشی است که قادر به اتصال به GDF-15 در گردش خون است و در نتیجه تعامل آن با گیرنده GFRAL را مهار میکند. در یک کارآزمایی کوچک فاز 1b با برچسب باز، 10 بیمار مبتلا به کاشکسی سرطانی و سطح بالای GDF-15 در گردش خون با پونسگروماب درمان شدند و بهبودهایی در وزن، اشتها و فعالیت بدنی نشان دادند، در حالی که سطح سرمی GDF-15 مهار شد و عوارض جانبی کم بود. بر این اساس، ما یک کارآزمایی بالینی فاز 2 را برای ارزیابی ایمنی و اثربخشی پونسگروماب در بیماران مبتلا به کاشکسی سرطانی با سطح بالای GDF-15 در گردش خون، در مقایسه با دارونما، انجام دادیم تا این فرضیه را که GDF-15 پاتوژنز اصلی بیماری است، آزمایش کنیم.
این مطالعه شامل بیماران بزرگسال مبتلا به کاشکسی مرتبط با سرطان (سرطان ریه سلول غیرکوچک، سرطان پانکراس یا سرطان کولورکتال) با سطح سرمی GDF-15 حداقل 1500 پیکوگرم در میلیلیتر، امتیاز وضعیت تناسب اندام کنسرسیوم تومور شرقی (ECOG) ≤3 و امید به زندگی حداقل 4 ماه بود.
بیماران ثبتنامشده بهطور تصادفی برای دریافت 3 دوز 100 میلیگرم، 200 میلیگرم یا 400 میلیگرم پونسگروماب یا دارونما، به صورت زیرجلدی هر 4 هفته با نسبت 1:1:1، انتخاب شدند. هدف اولیه، تغییر وزن بدن نسبت به شروع مطالعه در 12 هفته بود. هدف ثانویه کلیدی، تغییر از شروع مطالعه در نمره مقیاس فرعی بیاشتهایی کاشکسی (FAACT-ACS)، ارزیابی عملکرد درمانی برای بیاشتهایی کاشکسی، بود. سایر اهداف ثانویه شامل نمرات ثبت علائم کاشکسی مرتبط با سرطان، تغییرات پایه در فعالیت بدنی و نقاط پایانی راه رفتن بود که با استفاده از دستگاههای سلامت دیجیتال پوشیدنی اندازهگیری میشدند. حداقل زمان مورد نیاز برای استفاده از دستگاه از قبل مشخص شده است. ارزیابی ایمنی شامل تعداد عوارض جانبی در طول درمان، نتایج آزمایشهای آزمایشگاهی، علائم حیاتی و الکتروکاردیوگرامها بود. اهداف اکتشافی شامل تغییرات پایه در شاخص عضله اسکلتی کمری (سطح عضله اسکلتی تقسیم بر مربع قد) مرتبط با عضله اسکلتی سیستمیک بود.
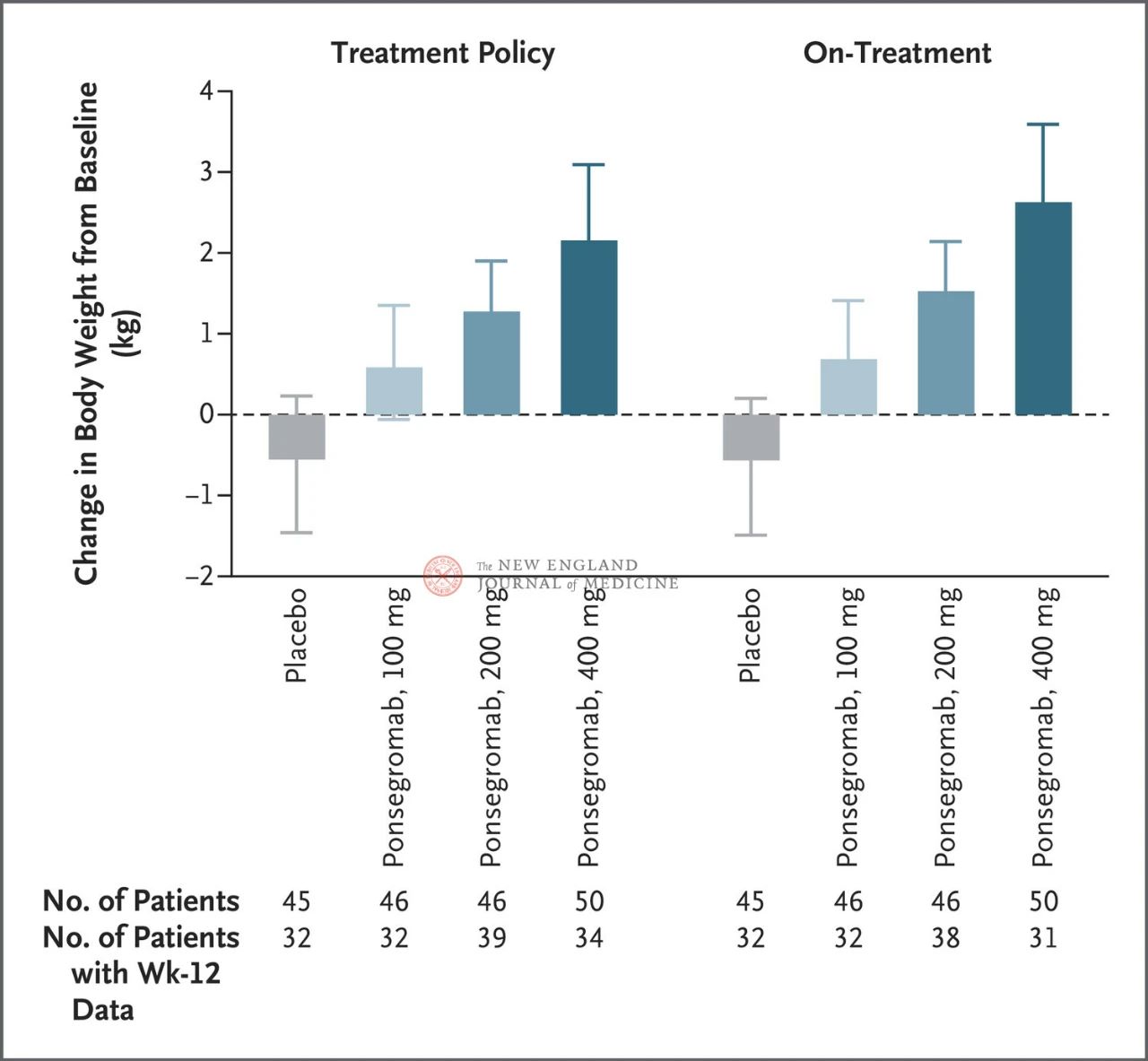
در مجموع ۱۸۷ بیمار به طور تصادفی برای دریافت پونسگروماب ۱۰۰ میلیگرم (۴۶ بیمار)، ۲۰۰ میلیگرم (۴۶ بیمار)، ۴۰۰ میلیگرم (۵۰ بیمار) یا دارونما (۴۵ بیمار) انتخاب شدند. هفتاد و چهار نفر (۴۰ درصد) مبتلا به سرطان ریه سلول غیرکوچک، ۵۹ نفر (۳۲ درصد) مبتلا به سرطان پانکراس و ۵۴ نفر (۲۹ درصد) مبتلا به سرطان کولورکتال بودند.
تفاوت بین گروههای ۱۰۰ میلیگرم، ۲۰۰ میلیگرم و ۴۰۰ میلیگرم و دارونما به ترتیب ۱.۲۲ کیلوگرم، ۱.۹۲ کیلوگرم و ۲.۸۱ کیلوگرم بود.
شکل، نقطه پایانی اولیه (تغییر وزن بدن از شروع مطالعه تا ۱۲ هفته) را برای بیماران مبتلا به کاشکسی سرطان در گروههای پونسگروماب و دارونما نشان میدهد. پس از تعدیل برای خطر رقابتی مرگ و سایر رویدادهای همزمان، مانند قطع درمان، نقطه پایانی اولیه با استفاده از نتایج هفته ۱۲ از یک تحلیل طولی مشترک بیزی (چپ) با استفاده از یک مدل Emax طبقهبندی شده تجزیه و تحلیل شد. نقاط پایانی اولیه نیز به روشی مشابه، با استفاده از اهداف تخمینی برای درمان واقعی، که در آن مشاهدات پس از تمام رویدادهای همزمان کوتاه شدند (شکل سمت راست)، تجزیه و تحلیل شدند. فواصل اطمینان (در مقاله نشان داده شده است)
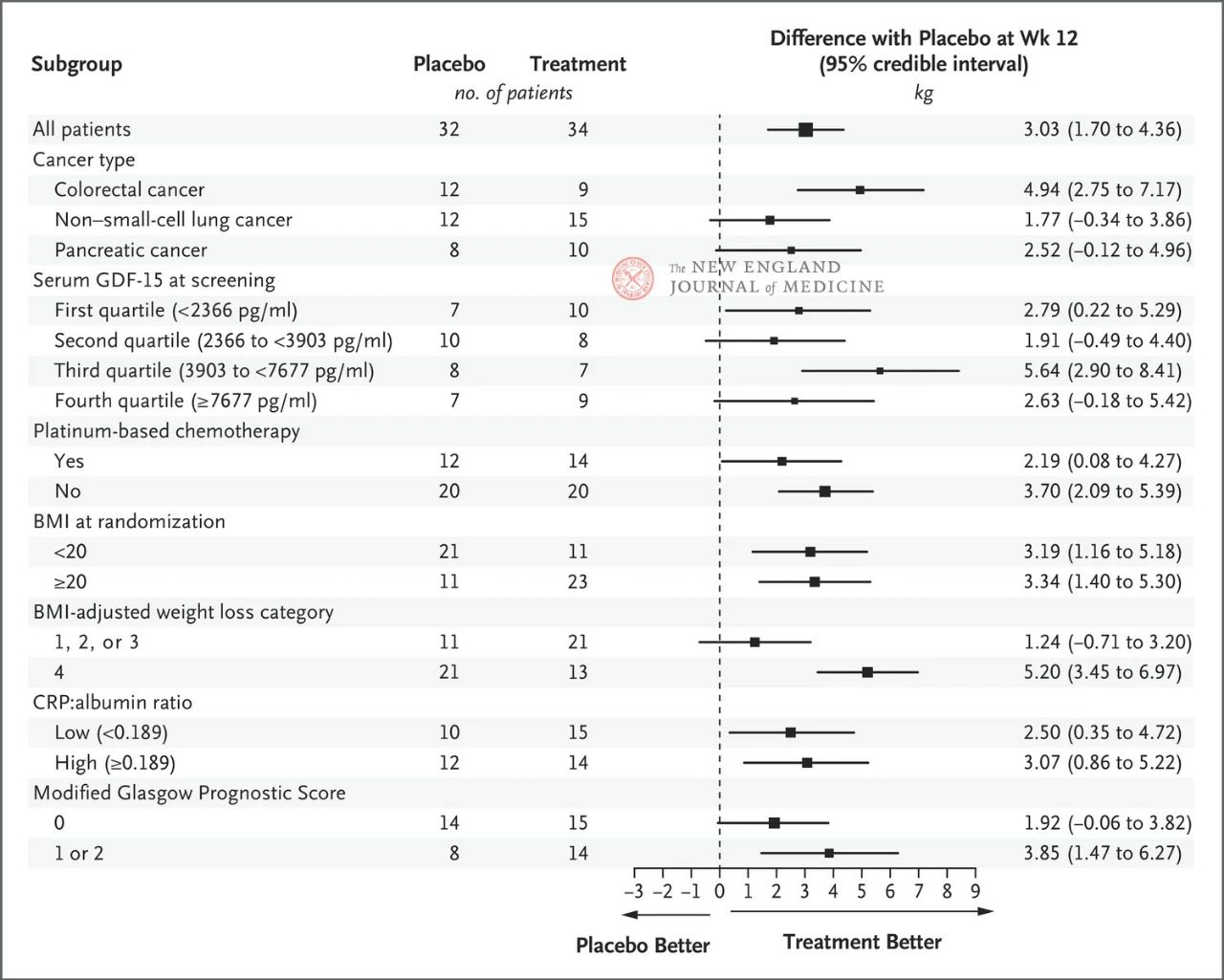
تأثیر ۴۰۰ میلیگرم پونسگروماب بر وزن بدن در زیرگروههای اصلی از پیش تعیینشده، از جمله نوع سرطان، چارک سطح سرمی GDF-15، قرار گرفتن در معرض شیمیدرمانی مبتنی بر پلاتین، شاخص توده بدنی (BMI) و التهاب سیستمیک پایه، ثابت بود. تغییر وزن با مهار GDF-15 در ۱۲ هفته سازگار بود.
انتخاب زیرگروههای کلیدی بر اساس یک تحلیل طولی مشترک بیزی پس از حادثه (post-hoc Bayesian joint lengthy analysis) انجام شد که پس از تعدیل خطر رقابتی مرگ بر اساس هدف تخمینی استراتژی درمانی انجام شد. فواصل اطمینان نباید به عنوان جایگزینی برای آزمایش فرضیه بدون تعدیلهای متعدد استفاده شوند. BMI نشان دهنده شاخص توده بدنی، CRP نشان دهنده پروتئین واکنشی C و GDF-15 نشان دهنده فاکتور تمایز رشد 15 است.
در شروع مطالعه، بخش بیشتری از بیماران در گروه پونسگروماب ۲۰۰ میلیگرمی هیچ کاهش اشتهایی را گزارش نکردند؛ در مقایسه با دارونما، بیماران در گروههای پونسگروماب ۱۰۰ میلیگرمی و ۴۰۰ میلیگرمی، بهبود اشتها را نسبت به شروع مطالعه در ۱۲ هفته گزارش کردند، که با افزایش نمرات FAACT-ACS به ترتیب ۴.۱۲ و ۴.۵۰۷۷ همراه بود. تفاوت معنیداری در نمرات FAACT-ACS بین گروه ۲۰۰ میلیگرمی و گروه دارونما وجود نداشت.
با توجه به الزامات زمان استفاده از پیش تعیینشده و مشکلات دستگاه، به ترتیب ۵۹ و ۶۸ بیمار دادههایی در مورد تغییرات در فعالیت بدنی و نقاط پایانی راه رفتن نسبت به شروع مطالعه ارائه دادند. در میان این بیماران، در مقایسه با گروه دارونما، بیماران گروه ۴۰۰ میلیگرم در ۱۲ هفته افزایش فعالیت کلی داشتند، با افزایش ۷۲ دقیقه فعالیت بدنی غیرکمتحرک در روز. علاوه بر این، گروه ۴۰۰ میلیگرم در هفته ۱۲ افزایش شاخص عضلات اسکلتی کمری نیز داشتند.
میزان بروز عوارض جانبی در گروه پونسگروماب 70٪ بود، در مقایسه با 80٪ در گروه دارونما، و در 90٪ از بیمارانی که همزمان درمان ضد سرطان سیستمیک دریافت میکردند، رخ داد. میزان تهوع و استفراغ در گروه پونسگروماب کمتر بود.
زمان ارسال: اکتبر-05-2024